解糖系
グルコースをエネルギーとして利用するには,細胞質内部だけで行える『解糖系』と,解糖系の産物であるピルビン酸を更にミトコンドリアの『クエン酸回路(TCA)』で燃焼させる経路とがあります.
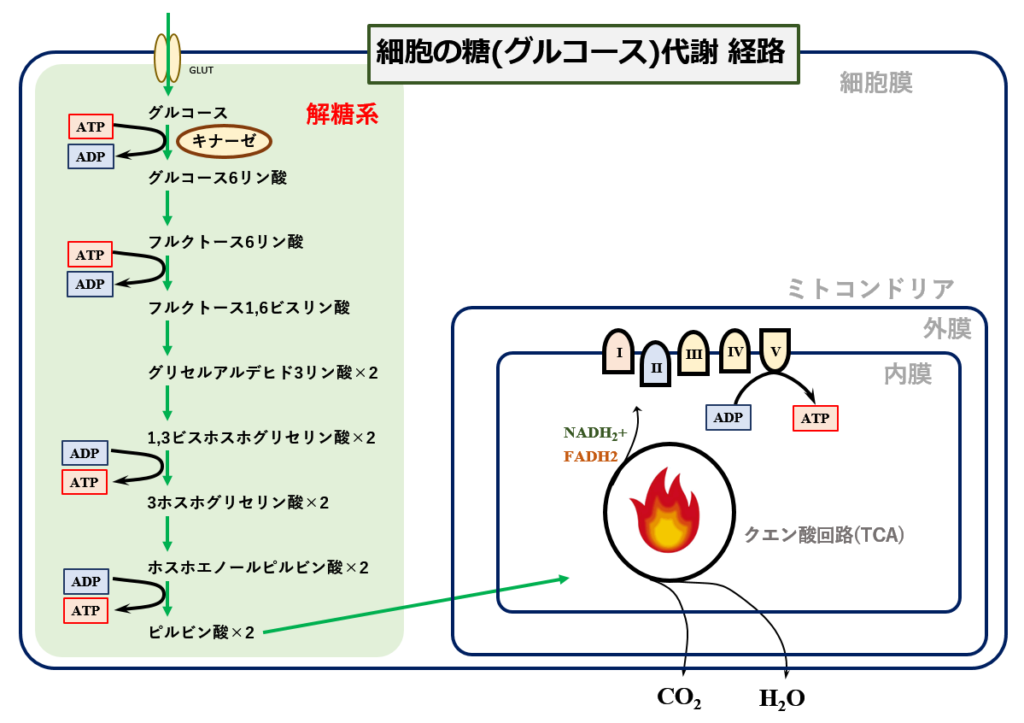
グルコース 1モルを完全に燃焼させると 674kcalの熱が発生しますが,ここまで完全に燃焼させられるのはミトコンドリアの力を借りた場合だけです.
グルコース→ 二酸化炭素 + 水 + 674 kcal
解糖系だけでは,グルコースからごく一部のエネルギーを取り出しているだけです.無酸素状態の解糖系ではグルコース1分子から2個のATPしか得られません.一方有酸素状態でミトコンドリア経由で完全燃焼させれば,32個のATPが産生されます[★]. 効率が段違いなのです.
[★] Harper 生化学 原書30版 表17-1 p.197
しかしながら,解糖系の利点は 酸素が存在しない場合,あるいは酸素供給が追い付かないような場合,すなわち無酸素状態でも進行できるという点です.したがって,激しい運動の時には解糖系が主役です.
速いけれど効率の悪い解糖系,遅いけれど無駄のないミトコンドリアのエンジン, 実にうまい組み合わせです.
そして,解糖系の先頭バッターで,グルコースにリン酸基を付加するのがグルコキナーゼなどです.
前回記事でグルコキナーゼ と書きましたが,実はこの役割を担うのはグルコキナーゼだけではありません. ヘキソキナーゼも同様に グルコースをリン酸化する酵素です.
もっと正確に言えば ヘキソキナーゼには[ヘキソキナーゼ1]から[ヘキソキナーゼ4]までの4種類があり,[ヘキソキナーゼ4]の別名がグルコキナーゼなのです.
- ヘキソキナーゼ1
- ヘキソキナーゼ2
- ヘキソキナーゼ3
- ヘキソキナーゼ4 = グルコキナーゼ
ヘキソキナーゼ
ヘキソキナーゼはこういう恰好をした酵素です.
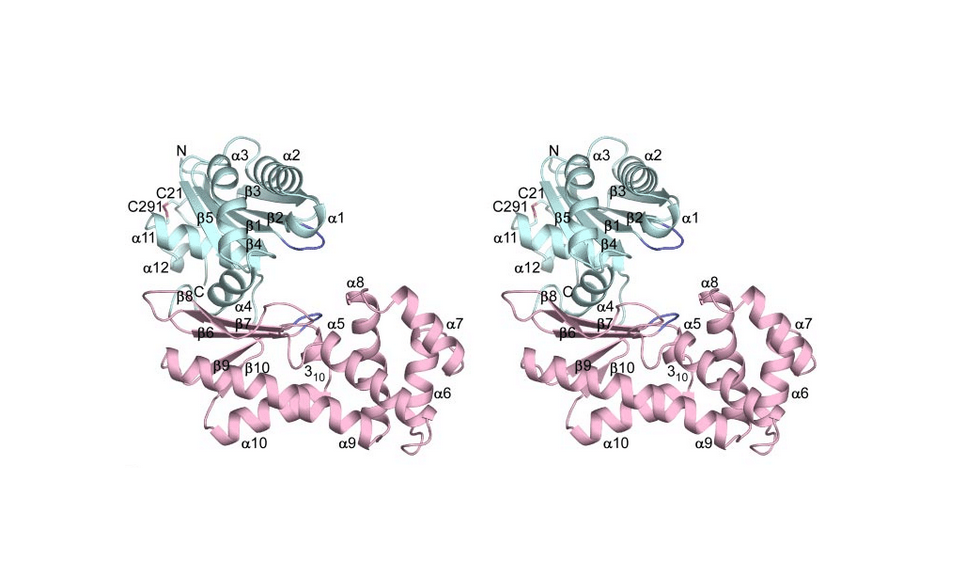
3D画像になっていますので,立体視のできる方であれば,よりリアルに構造がわかると思います.
水色の上半分と,ピンクの下半分とで包み込まれるような空間が形成されており,ここにグルコースとATPとを抱え込む,しかも両者の反応する部分がピタリと向かい合うように抱えこんでおいてから,ATPから有無を言わさずリン酸基を一つ奪ってグルコースにくっつけてしまいます.
単にグルコースとATPとを水に溶かしてビーカーに入れただけでは いつまで待ってもこの反応はほとんど起こりません. しかし この酵素=ヘキソキナーゼが存在していると,両者を原子レベルで極めて狭い空間に最適の姿勢にして押さえ込むので 反応は速やかに進行します.
無酸素運動時の主力エンジンなのですから,解糖系の第一ステップである,このヘキソナーゼによるリン酸化には高速動作が要求されます.
実際,筋肉細胞に存在する ヘキソキナーゼI (又はII)の動作特性はこうなっています.
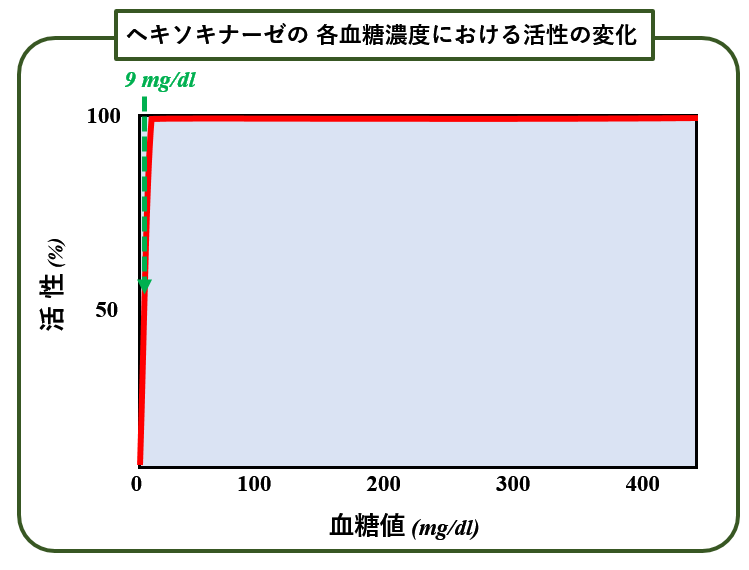
縦軸はヘキソキナーゼがグルコースにリン酸基をくっつける反応の速度(最大速度=100とする),そして横軸は その時のグルコース濃度(=血糖値)です.
ご覧の通り,血糖値が9mg/dlという ほとんどゼロに近いような低血糖状態であっても,あるいは400mg/dlを越える高血糖状態でも, ヘキソキナーゼは グルコースを見つけると無条件に捕まえてリン酸化してしまうのです.
[続く]

コメント