本題の前に トピックスです
前回記事で;
[密閉空間]+[長時間]+[接近]の3条件が感染リスクを高める
と書きましたが,まさにこの条件通りの感染事例が韓国で発生したようです.
新型肺炎感染者31人追加…計82人に[韓国:中央日報 2020年2月20日 10:38]
韓国:大邱市のキリスト教会で,1人の感染源から,一挙に23人に感染したようです. この教会では,大人数が密集して集団ミサを行うのが通例だったようです.

新型コロナウイルスはどのように重篤化していくのか
新型コロナウイルス罹患により,重篤な肺炎・呼吸困難が生ずることがありますが,それが人体組織のどのような病変によるものか,未だ概要すら把握しきれておりません. 現時点では,医療関係者のすべてのエネルギーを感染拡大防止と治療に振り向けるのが精一杯だからです. そんな中,2月17日に中国の科学者によって,新型コロナウイルス(COVID-19)で死亡に至った中国の患者の死後解剖所見から,この感染症が病理学的にどのように進行するのか貴重な報告が発表されました. The Lancet Onlineに 2月17日 掲載された 短報です.

原文の機械翻訳から作成した抄訳を紹介します.
経緯
2020年1月21日:
50歳の男性が発熱,悪寒,咳,疲労,息切れを主訴として発熱クリニックに入院.
患者は1月8〜12日に武漢に旅行歴があり,1月14日(=発症1日目とする)に軽度の悪寒と乾いた咳の初期症状があったものの,病院には行かず1月21日まで働き続けていた.
胸部X線にて,両肺に複数の斑状の陰影を認めたため,咽頭スワブを採取した.
2020年1月22日(発症9日目):
北京疾病管理センター(CDC)は,患者がCOVID-19陽性であることをrt-PCRによって確認.
直ちに隔離病棟に入院させ,フェイスマスク越しに酸素補給を開始.
抗ウイルス療法としてインターフェロンアルファ-2b(1日2回500万単位,噴霧吸入)とロピナビル+リトナビル(1日2回500 mg,経口),および二次感染を防ぐためにモキシフロキサシン(1日0.4 g,静脈内)を投与.
深刻な息切れと低酸素血症を考慮して,肺炎症を抑えるためにメチルプレドニゾロン(80 mgを1日2回,静脈内)も投与.
投薬開始後,体温は39°Cから36°Cに低下. しかし,咳,呼吸困難,疲労は改善せず.
2020年1月25日(発症12日目):
最初の症状が現れた後,胸部X線写真では,両方の肺に進行性の浸潤と拡散性のグリッド影をみとめた.患者は閉所恐怖症のため,ICUでの人工呼吸器のサポートを繰り返し拒否した.そのため,高流量鼻カニューレ(HFNC)酸素療法(60%濃度,流量40 L /分)を適用した.
2020年1月26日(発症13日目):
患者の症状は改善しないが,酸素飽和度は95%以上を保っていた.
2020年1月27日(発症14日目):
同日午後,低酸素血症と息切れが悪化. HFNC酸素療法(100%濃度,流量40 L / min)としたにもかかわらず,酸素飽和度は60%に低下し,突然心停止した.直ちに侵襲的換気,胸部圧迫,およびアドレナリン注射を行ったものの,残念ながら救命にはいたらず,18:31(北京時間)死亡した.
死後剖検
生検サンプルを,患者の肺,肝臓,心臓組織から採取した.
組織学的検査では,細胞性線維粘液様滲出液による両側びまん性肺胞損傷が示された. 右肺は,肺細胞の明白な落屑と硝子膜の形成を示し,急性呼吸窮迫症候群を示していた. 左肺組織は,初期段階のARDSを示唆するヒアリン膜形成を伴う肺水腫を示した. リンパ球が優勢な間質性単核炎症性浸潤物が両方の肺に見られた. 大きな核,両親媒性顆粒細胞質,顕著な核小体を特徴とする異型拡大肺細胞を伴う多核合胞体細胞が肺胞内空間で同定され,ウイルス性細胞変性様変化を示した. 核内または細胞質内の明らかなウイルス封入体は確認されなかった.
COVID-19の病理学的特徴は,SARSおよび中東呼吸器症候群(MERS)コロナウイルス感染症で見られるものと非常に似ている.さらに,COVID-19患者の肝生検標本は,中程度の微小血管脂肪症と軽度の小葉および門脈を示していた.これは,SARS-CoV-2感染または薬物誘発性肝損傷のいずれかによって損傷が引き起こされた可能性があることを示している.いくつかの間質性単核炎症性浸潤があったが,心臓組織に他の実質的な損傷はなかった.末梢血は,フローサイトメトリー分析にかけられた. HLA-DR(CD4 3・47%)およびCD38(CD8 39・4%)の割合が高いことから明らかなように,末梢CD4およびCD8 T細胞の数は大幅に減少し,その状態は過剰に活性化されていた. CD4 T細胞では炎症性の高いCCR4 + CCR6 + Th17の濃度が増加していた.さらに,CD8 T細胞は高濃度の細胞傷害性顆粒を保有していた.31.6%の細胞はパーフォリン陽性,64.2%の細胞はグラニュリシン陽性,30.5%の細胞はグラニュリシンおよびパーフォリン二重陽性であった.この結果は,Th17の増加とCD8 T細胞の高い細胞毒性によって明らかになったT細胞の過剰活性化が,この患者の重度の免疫損傷の一部を占めていることを示唆している.
結論
リンパ球減少症はCOVID-19患者の一般的な特徴であり,疾患の重症度と死亡率に関連する重要な要因である可能性がある.
本報告のCOVID-19重篤症例における臨床的および病理学的所見は,死因の特定に役立つだけでなく,SARS-CoV-2関連肺炎の病因に関する新たな洞察を提供し,医師が同様の重症患者に対して適切な治療戦略をたてる一助となって死亡率の低下に結びつけられる可能性がある.
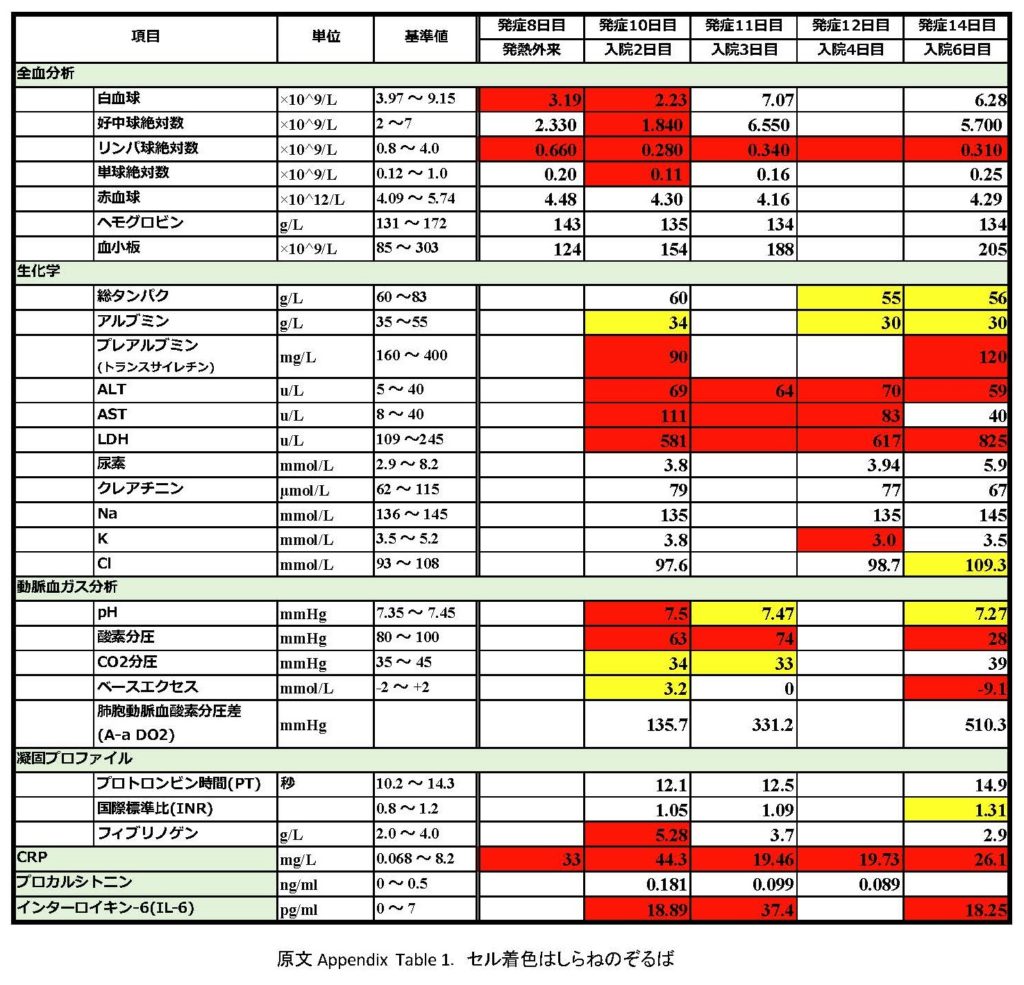
入院中の検査数値の推移
感想
以下は文献内容ではなく,しらねのぞるばの感想です.
呼吸器官系の用語には詳しくないので,翻訳には間違いが多いかもしれません.
この詳しい組織解剖検査と検査数値の推移から,やはり新型コロナウイルスは,免疫をつかさどるリンパ球が減少(=入院2日目にリンパ球が急減)から始まり,数が少なくなった CD8 T細胞が数の少なさを活性過激化で補おうとしたために肺細胞を攻撃し,肺機能が失われて呼吸困難に陥っていくことが示されました.
人体の免疫は ヘルパーT細胞とキラーT細胞によって成り立っていますが,前者が消防車による消火活動だとすれば,後者は江戸時代の「火消し」でしょう.江戸時代の火消しは,消火自体はあきらめて,その代わり延焼を防ぐために,火事の周囲の家を壊していくように,キラー細胞は,感染細胞を死滅させてそれ以上の感染拡大を防いでいくのです.しかし 上記の報告にもあるように,キラーT細胞(CD8)が過剰に細胞破壊を続けたために,炎症指標(CRP, IL-6)が悪化し,ついには100%の酸素の大量(40L/分)吸入でも呼吸不能となって患者の死に至ったようです.
ウイルスは免疫を壊しているだけであり,死に至るほどの呼吸困難を引き起こしているのは,実は人体自身の免疫細胞であるというのは,実におそろしいです. このウイルスが人工のものではないかという噂が出回るのも無理がないと思いました.


コメント
非常にわかりやすい翻訳と解説、ありがとうございました。
自己免疫疾患とも言えるような状況になるわけですね・・・
> 自己免疫疾患とも
そうですね. ただ自己免疫疾患の場合は,免疫系が登場する必要がないのに過剰応答しているのに対して,このコロナの場合は,免疫系自体が『手負いの獅子』になって暴れまくっている,という違いでしょうか.